Allogen stamcelletransplantasjon er en behandlingsform ved sykdommer i blod og benmarg. Allogen betyr at en overfører stamceller fra et annet individ. Før en transplantasjon gis en forbehandling. Benmargsutryddende (myeloablativ) forbehandling har til hensikt å utrydde pasientens egen benmarg, for å drepe kreftceller og lage plass til ny benmarg. Samtidig hemmes pasientens immunforsvar (immunologisk effekt mot gjenværende leukemiceller), slik at faren for avstøting av de fremmede stamcellene reduseres. Blodproduserende stamceller overføres fra et individ som vanligvis er vevstypeidentisk, men forøvrig genetisk forskjellig fra pasienten.
Pasienten må ikke ha alvorlig kompliserende sykdom, og det må foreligge en egnet giver (donor). Ved bruk av familiegiver er transplantasjon med benmargsutryddende forbehandling aktuelt til pasienter under cirka 60 år. Komplikasjonsrisikoen er større når ubeslektet donor benyttes. Ubeslektet, vevstypeidentisk giver er aktuelt for utvalgte pasienter under cirka 55–60 år. Man forsøker å ta hensyn til pasientens biologiske alder. Dersom man kan velge mellom flere givere foretrekkes vanligvis donor av samme kjønn som pasienten.
Behandlingen kan helbrede ellers uhelbredelige blodsykdommer, men den er så kraftig at den er forbundet med mye plager, og det er en risiko for at pasienten kan å dø av komplikasjoner.
Transplantasjon av stamceller med benmargsutryddende forbehandling gjøres ved:
- Akutt myelogen leukemi (AML):
- i første remisjon til pasienter som ikke har lav risiko for tilbakefall, dersom pasienten er under cirka 60 år og familiegiver finnes.
- etter tilbakefall, ved begynnende første tilbakefall og i senere, fortrinnsvis, annen remisjon.
- hos pasienter under cirka 60 år med høy risiko for tilbakefall med egnet ubeslektet giver i første remisjon.
- Akutt lymfatisk leukemi (ALL):
- i første remisjon med høyrisikokriterier og ved i ny remisjon etter første tilbakefall.
- Kronisk myelogen leukemi (KML):
- Benmargskreft (myelomatose)
- Annet
Les mer om stamcelletransplantasjon med forbehandling
Donor
Helst ønsker man å bruke familiegiver, og for tiden kan familiegiver med inntil ett ikke-identisk (uforlikelig) humant leukocyttantigen (HLA) brukes.
Dersom pasienten ikke har familiegiver vil man vurdere om ubeslektet giver med identisk vevstype kan brukes. Ubeslektede givere vil til tross for likhet ved undersøkelser likevel kunne ha små forskjeller i sine HLA-molekyler, som er av betydning for transplantat-mot-vert-sykdom og forkastelsesreaksjoner. Ved ubeslektede givere gjøres derfor en utvidet (genomisk) vevstyping.
Stamcelletransplantasjon for akutt og kronisk myelogen leukemi med benmarg fra HLA-genidentiske ubeslektede givere har hos yngre pasienter gitt nesten like gode resultater som ved bruk av stamceller fra familiegivere. Komplikasjonsrisikoen er større og øker med alderen.
Dersom man ikke finner giver til pasienten kan det en sjelden gang være aktuelt å lete etter navlestrengsblod som stamcellekilde.
Stamcellehøsting
Bloddannende stamceller kan skaffes til veie ved å suge ut benmarg fra giverens hoftekam eller ved å "mobilisere" blodproduserende stamceller fra benmarg til blod. Mobiliseringen gjøres ved hjelp av bloddannede vekstfaktorer, oftest granulocytt-kolonistimulerende faktor (G-CSF) som gis til pasienten. Vekstfaktorene påvirker antagelig adhesjonsmolekyler på stamcellene og benmargsstroma (ikke-blodproduserende benmarg) slik at stamcellene løsner og kommer ut i blodsirkulasjonen. På grunn av denne teknikken har det blitt vanlig å snakke om stamcelletransplantasjon i stedet for benmargstransplantasjon, fordi det gjenspeiler begge måtene å høste stamceller på.
Høsting av benmarg
Ved bruk av stamceller fra benmarg får den vevstypeidentiske donor vanligvis full narkose og legges i bukleie. Benmarg suges ut med hjelp av gjentatte nålestikk gjennom hoftekammen. Inngrepet varer totalt i 1 time i gjennomsnitt. Benmargsmaterialet med stamcellene overføres til blodposer tilsatt heparin (blodfortynnende medikament), slik at koagulering (blodlevring) unngås.
Høsting fra blod
Ved høsting av stamceller fra blod trenger ikke giveren narkose, men prosedyren kan være relativt tidkrevende. Stamcellene høstes vanligvis fra en perifer vene i underarm, ved hjelp av en spesiell maskin som separerer stamcellene (leukaferese).
Hver leukaferese tar mange timer. Det er nødvendig med 1–3 leukafereser.
Det er gode holdepunkter for at bruk av stamceller fra blod kan gi raskere gjenoppretting av bloddannelsen enn stamceller fra benmarg.
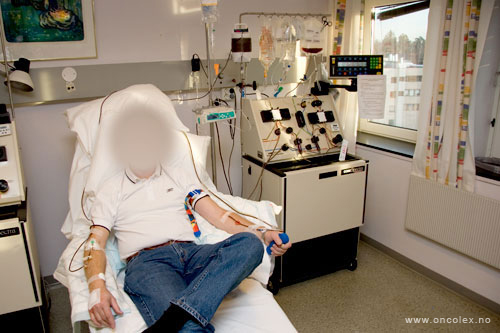
Ved høsting av stamceller fra
blod trenger ikke giveren
narkose, men prosedyren kan
være relativt tidkrevende.
Stamcellene høstes fra en
perifer vene.

En leukaferesemaskin
sentrifugerer blodet og
skiller de ulike
blodkomponentene
fra hverandre.
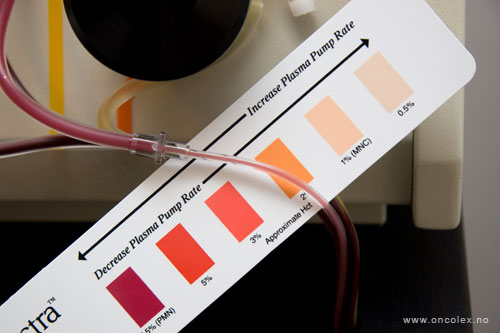
Et fargekart brukes for å
sikre at det hovedsaklig
er hvite blodceller med
stamceller som samles
i en pose.

Plasma (venstre slange)
og blodceller (høyre slange)
blandes og returneres
til giveren.
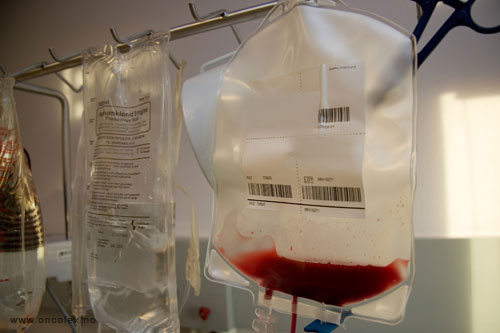
Stamcellene samles
i en pose. Cellene gis
direkte eller fryses
ned for senere bruk.
Forberedelser
Søknad om transplantasjon rettes til Den norske gruppen for allogen stamcelletransplantasjon. Her gis nødvendig informasjon om sykdom, behandling som er gitt og forløp fram til henvisning og pasientens tilstand, samt om pasienten har potensiell familiedonor.
Pasient og pårørende får grundig informasjon om behandling, komplikasjoner og praktiske forhold som bør ordnes i forkant av behandlingen. Pasienten vil også få tilbud om samtale med en tidligere stamcellestransplantert pasient.
Utredning i forkant av transplantasjon
I tillegg til ulike blodprøver og benmargsprøve er det en rekke undersøkelser som alle pasienter må igjennom før stamcelletransplantasjon.
- Lungefunksjonsprøver
- Tannlegeundersøkelser
- Sædundersøkelse/undersøkelse ved kvinneklinikken
- Øyeundersøkelse
- Røntgenundersøkelse av hjerte og lunger, eventuelt andre røngtenundersøkelser.
Nedfrysning av sæd/eggstokkvev
Det er viktig å tilby menn nedfrysning av sæd hvis det er praktisk mulig før cellegiftbehandling av en alvorlig sykdom. Det er realistisk å regne med at pasienten etter transplantasjon vil bli steril.
Nedfrysning av eggstokkvev er teknisk mulig, men bruk av slikt vev er per i dag eksperimentelt.
Forberedelser til stamcelletransplantasjon
Før man starter opp forbehandlingen er det en del tiltak som må gjøres for å forebygge og behandle komplikasjoner av cellegiftbehandling og transplantat-mot-vert-sykdom.
Behandling med blodprodukter
Alle blodprodukter som gis i tidsrommet fra 1 måned før transplantasjonen til minst 12 måneder etterpå, må være bestrålt for å hindre at eventuelt medfølgende T-lymfocytter slår seg ned og formerer seg hos den immunsupprimerte pasienten, med transplantat-mot-vert-sykdom som resultat. Bestråling er nødvendig til tross for at man alltid bruker blodprodukter fri for hvite blodceller. Alle pasienter skal ha leukocyttfiltrerte blodprodukter.
Infeksjonsforebyggende behandling
Det gis infeksjonsforebyggende behandling med antibiotika, antivirusmidler og behandling mot soppinfeksjon.
Forebyggende behandling mot transplantat-mot-vert-sykdom
Ciklosporin og metotreksat gis rutinemessig som forebyggende behandling mot akutt og kronisk transplantat-mot-vert-sykdom. Andre behandlingsopplegg er også i bruk.
Forebygging av tilbakefall til sentralnervesystemet
Ved akutt lymfatisk leukemi gis vanligvis tilførsel av cellegift (metotreksat) i ryggmargsvæske i to omganger som del av forbehandlingen, for å forebygge leukemi i sentralnervesystemet.
Gjennomføring
Benmargsutryddende forbehandling
Ved ondartede blodsykdommer vil pasienten i løpet av de siste 8 døgn før transplantasjonen vanligvis få høydosebehandling med kombinasjonen busulfan i 4 dager og deretter cyklofosfamid i 2 dager. Noen få pasienter som ikke klarer å ta busulfan gjennom munnen får et intravenøst busulfanpreparat. Hos pasienter som har hatt tilbakefall av akutt leukemi til hjerne/ryggmarg kan total bestråling av sentralnervesystemet være aktuelt før de øvrige medikamentene gis.
I spesielle tilfeller er det aktuelt å gi helkroppsbestråling og cyklofosfamid.
Forebygging av betennelse i blæreslimhinne
Nedbrytningsprodukter av cellegifter lager sår og betennelse i slimhinnen i blæren, som kan blø (hemorragisk cystitt). For å forebygge dette gis:
- Rikelig væsketilførsel starter før første dose busulfan (eller cyklofosfamid ved helkroppsbestråling). Væsken gis kontinuerlig intravenøst med samtidig måling av vannlatning. Væskebehandlingen stoppes cirka 20 timer etter siste infusjon med cyklofosfamid.
- Mesna gis forebyggende for å beskytte urinveiene i forbindelse med tilførsel av cyklofosfamid.
Kvalmeforebyggende og -behandling
Kvalmeforebyggende medikamenter gis før behandling med cellegift.
Tilførsel av stamceller
Stamcellene tilføres mottakeren gjennom blodet, som ved en vanlig blodoverføring, eller i støt (som ved HMAS) dersom stamcellene har vært frosset ned.
Stamcellene finner frem til mottakerens margrom hvor de slår rot, blant annet ved hjelp av adhesjonsmolekyler, og deler seg (formerer seg) i et komplisert og ennå langt fra fullstendig klarlagt samspill mellom ulike cytokiner, vekstfaktorer og cellulære interaksjoner.
I løpet av 2–4 uker vil granulocytter begynne å vise seg i pasientens perifere blod. Effektiv blodplateproduksjon kommer som regel i gang noe senere.
Ved ikke-identisk blodtype (ABO-uforlik) mellom giver og mottaker kan det oppstå alvorlig nedbrytning av røde blodceller (hemolyse). For å forhindre dette er det aktuelt å fjerne røde blodceller fra transplantatet og/eller antistoffer fra pasienten og/eller transplantatet.

Stamcellene fraktes til
avdelingen i en beholder
som har temperatur
på -135 grader Celsius.

Stamcellene varmes opp
i vannbad til 38 grader
Celsius.
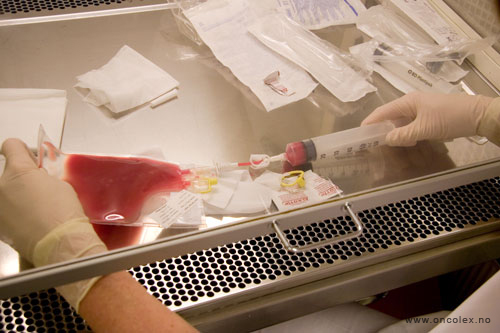
Stamcellene trekkes opp
i en sprøyte og gis
umiddelbart til pasienten.
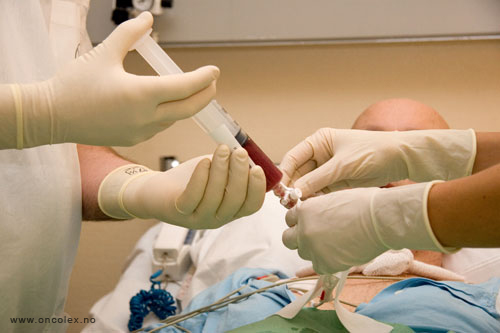
Stamcellene settes i en
kateter som går direkte
inn i blodbanen.
Pasienten overvåkes med
tanke på eventuelle
allergiske reaksjoner.
Oppfølging
I de første ukene etter stamcelletransplantasjonen står pasienten i stor fare for å få infeksjoner, særlig bakterielle. Pasienten oppholder seg i beskyttende isolat med overtrykksventilasjon og filtrert luft fra 5. dag etter transplantasjonen. Isolatet oppheves når granulocytter er stabilt (over 0,2 x 109/l i minst 3 dager sammenhengende, av og til lengre).
I den periode pasienten er isolert følger både pasient, pårørende og helsepersonell egne rutiner for å redusere infeksjonsfaren. Enkelte rutiner gjøres daglig i påvente av at den nye margen skal begynne å fungere. Hensikten med å følge rutinene er å forebygge komplikasjoner og sikre at eventuelle komplikasjoner oppdages tidlig.
Daglig tas blodprøver, rektal temperatur, puls og blodtrykk. Vekt og væskebalanse måles, og det gjøres inspeksjon av munn, hals og hud.
Ved komplikasjoner er det viktig at behandlingen raskt kan settes i gang.
Blodoverføring av blodplater og røde blodceller
Blodoverføring av blodplater og røde blodceller er nødvendig i flere uker etter transplantasjonen for å holde platetall og hemoglobin på et forsvarlig nivå. For å forebygge transplantat-mot-vert-sykdom brukes kun bestrålte blodprodukter.
Ikke-identisk ABO-blodtype
Ved stamcelletransplantasjon med giver med ikke-identisk ABO-blodtype, gis etter transplantasjonen røde blodceller av type O inntil pasienten har skiftet til donors blodtype.
Ernæring
Cellegiftbehandlingen forårsaker som regel kvalme og oppkast. Medikamenter kan også påvirke smaken og nedsette apetitten i dager og uker. De fleste pasienter får i tillegg såre slimhinner i munnen med tildels betydelige smerter etter den kraftige cellegiftbehandlingen.
Pasientens ernæringsstatus overvåkes og behovet for ernæring gjennom blodet (total parenteral ernæring) vurderes individuelt. Nesten alle pasienter trenger ernæring via blodet en periode etter forbehandlingen og i perioden hvor benmargsfunksjonen er kraftig nedsatt (aplasifasen).
Såre slimhinner
Såre slimhinner i munn, tarmslimhinne og andre slimhinner oppstår ofte samtidig med at blodverdiene er på sitt laveste. Det er individuelt hvor sår man blir i munnen. Såre slimhinner i munnen er både en inngangsport for bakterier, og kan også være smertefullt. Det gjøres forbyggende munnstell under hele behandlingen. Smertene såre slimhinner medfører behandles med smertestillende medikamenter.
Ved såre slimhinner i endetarmen smøres pasienten godt. Ved avføring kan det være lurt å bruke mykt toalettpapir med jordnøttolje på og smøre godt nedentil etter hvert toalettbesøk. Grønnsåpebad virker lindrende.
Diaré
Pasienter som har fått kraftig cellegiftbehandling og/eller total kroppsbestråling får som regel diaré. Dette skyldes at behandlingen gir skade av tarmslimhinnen, som er forbigående. Diaréen kan forventes å vare under og i flere uker etter gitt behandling.
Transplantat-mot-vert-sykdom kan også gi kraftig diaré. Denne diaréen kan eventuelt komme noen uker etter transplantasjonen, omtrent når man kan forvente at kroppen aksepterer transplantatet, men også senere i forløpet.
Kraftig og bredspektret antibiotikabehandling i perioden hvor benmargsfunksjonen er betydelig nedsatt, vil kunne gi endringer i tarmfloraen med diaré. Pasienter er også utsatt for smitte fra næringsmidler inntatt peroralt.
Ernæringstilstanden kan som regel kontrolleres ved at pasienten får ernæring via blodet, med tilskudd av væske, elektrolytter og proteiner. Ernæring via sonde er aktuelt, men kan være vanskelig å gjennomføre.
Komplikasjoner
Man forventer en del komplikasjoner etter transplantasjonen. Komplikasjoner kan noen ganger være alvorlige og livstruende og i verste fall dødelige.
Infeksjoner
På grunn av store doser med busulfan og cyklofosfamid får pasientene en alvorlig immundefekt og lavt antall hvite blodceller (granulocytter) i løpet av få dager etter medikamenttilførsel.
Ved alvorlig lavt antall hvite blodceller vil vanlige infeksjonstegn ofte mangle. I perioden hvor benmargsfunksjonen er betydelig nedsatt dreier det seg nesten alltid primært om bakterielle infeksjoner, som raskt kan bli meget alvorlige. Eneste infeksjonstegn er ofte feber, som derfor må tas meget alvorlig hos denne type pasienter.
Blir pasienten feberfri av antibiotikabehandlingen bør behandlingen likevel fortsette i minst 3 dager (eller til granulocyttallet er over 0,2 x 109/l).
Både forebyggende behandling mot transplantat-mot-vert-sykdom og eventuell transplantat-mot-vert-sykdom, som trenger behandling med steroider eller andre immundempende medikamenter, øker immundefekten. Selv etter at pasienten har fått tilstrekkelig hvite blodceller, er infeksjonsforsvaret fortsatt svekket, med betydelig fare for infeksjoner.
Mikrober som kan gi livstruende opportunistiske infeksjoner er cytomegalovirus (CMV), sopp (særlig candida og aspergillus), pneumocystis jerovecii og ulike bakterier.
Soppinfeksjon
De aller fleste pasienter får soppforebyggende middel (fluconazole) mot candidainfeksjon fra dagen før transplantasjonen til dag 75. Hos pasienter som i fasen hvor benmargsfunksjonen er betydelig nedsatt (aplastisk fase) har fått antibiotika i 5–7 døgn uten å bli feberfri, eller som får ny temperaturstigning tross adekvat antibiotikabehandling, må man anta at det foreligger en utbredt soppinfeksjon, særlig dersom annen infeksjon ikke kan påvises. Eventuelt vurderes annen soppbehandling enn fluconazole.
Lungebetennelse/pustebesvær
Fortetninger på lungene skyldes oftest enten bakterie- eller soppinfeksjon. Det er viktig å være oppmerksom på at pasienter uten granulocytter sjelden utvikler tydelige fortetninger. Røntgen av lungene viser oftest ingen funn i fasen hvor benmargsfunksjonen er betydelig nedsatt, og høyoppløselig CT er en langt mer sensitiv undersøkelse.
Interstitiell lungebetennelse
Interstitiell lungebetennelse er en betennelse i lungevev med tallrike små utbredte infeksjonsområder. Tilstanden er en fryktet komplikasjon hos stamcelletransplanterte pasienter. Interstitiell lungebetennelse kan oppstå både før og i mange måneder etter at de tilførte stamcellene har etablert seg i benmargen. Dødeligheten er høy. Tilstanden kan blant annet skyldes infeksjoner som er tilgjengelige for behandling, som for eksempel cytomegaloinfeksjon (virus) og pneumocytis jerovecii (sopp).
Det er meget viktig å komme raskt i gang med riktig behandling. Pasienter med interstitiell lungebetennelse kan raskt bli respiratortrengende og pasientens tilstand må følges nøye med måling av oksygenmetning (pulsoksymeter) og måling av oksygen, karbondioksid og surhetsgrad i arterielt blod.
Cytomegaloinfeksjon
Cytomegaloinfeksjon (CMV) er ikke uvanlig etter allogen stamcelletransplantasjon og skyldes oftest nye virusutbrudd (reaktivering) hos pasienter som har en latent virusinfeksjon. Akutt transplantat-mot-vert-sykdom og behandling av denne øker risikoen.
Infeksjonen kan vise seg via lave antall blodplater og lave antall hvite blodceller, uforklart feber, eventuelt leverbetennelse eller mage-tarmsymptomer til livstruende betennelse i lungevev.
CMV-pneumonitt oppstår typisk 40–60 dager etter transplantasjon, men forekommer også senere i forløpet. Frykten for CMV-pneumonitt er en av årsakene til at man bruker blodprodukter som er filtrert for hvite blodceller ved allogen stamcelletransplantasjon.
Ved påvist CMV-infeksjon (positiv pp65 eller CMV-PCR) gis vanligvis antivirusbehandling (ganciclovir).
Les mer om infeksjoner
Akutt transplantat-mot-vert-sykdom
Transplantat-mot-vert-sykdom er en tilstand der T-lymfocytter fra giver angriper celler og vev hos pasienten. Transplantat-mot-vert-sykdom er den viktigste komplikasjonen til allogen stamcelletransplantasjon. Sykdommen angriper hud og/eller tarm og/eller lever. Forebygges ved demping av infeksjonsforsvaret (immunsuppresjon), vanligvis ved ciklosporin. Pasienten behandles med kortikosteroider og eventuelt andre immunsuppressive medikamenter. Forløpet er i verste fall dødelig og risikoen for opportunistiske infeksjoner betydelig.
Benmargssvikt
Benmargssvikt vil si vedvarende anemi (lavt antall røde blodceller), lavt antall hvite blodceller og lavt antall blodplater. Årsaker til benmargssvikt kan være:
- avstøting av benmarg (sjelden)
- sen etablering av tilførte stamceller i benmargen (slik at produksjon av nye blodceller ikke kommer igang)
- infeksjon (blant annet cytomegaloinfeksjon)
- medikamenter som påvirker benmargen
- transplantat-mot-vert-sykdom
Megakaryocyttfunksjonen gjenopprettes ofte sist etter stamcelletranplantasjon. Lavt antall blodplater kan også skyldes økt forbruk av blodplater på grunn av for eksempel infeksjon, transplantat-mot-vert og andre immunologiske prosesser.
I tilegg til sviktende benmargsfunksjon kan anemi skyldes blødninger og/eller nedbrytning av røde blodceller (hemolyse). Ved ikke-identisk ABO-blodtype ses av og til betydelig forsinkelse av tilstrekkelig dannelse av røde blodceller (opptil over ett år).
Langvarig nedsatt matlyst
Langvarig nedsatt matlyst (anoreksi) kan blant annet skyldes infeksjon, transplantat-mot-vert-sykdom, leverforstyrrelser og medikamenter. Dersom pasienten i tillegg har svelgbesvær må man tenke på betennelse i spiserøret, eventuelt betennelse i magesekken eller magesår. Ernæringstilstanden skal ved behov opprettholdes med intravenøs ernæring som i seg selv kan gi anoreksi hos enkelte pasienter.
Blærebetennelse
Blærebetennelse (hemorragisk cystitt) som følge av høye doser cyklofosfamid, eventuelt høye busulfandoser kan oppstå. Til tross for forebyggende behandling med væsketilførsel og mesna, som virker beskyttende på nyre/urinveier ved cellegiftbehandling, får en del pasienter allikevel symptomer som blod i urinen, smertefull vannlatning og hyppig vannlatning. Symptomene kommer som regel under eller i løpet av de første dagene etter cyklofosfamid-infusjon. Enkelte pasienter kan utvikle blærebetennelse senere i forløpet, muligens som en manifestasjon av transplantat-mot-vert-sykdom, men også som en følge av virusinfeksjon.
Behandlingen er å fortsette eller gjenoppta væsketilførsel/måling av vannlatning. Eventuelt gis smertestillende og antivirusbehandling.
Venookklusiv leversykdom (VOD)
Denne tilstandens skyldes cellegiftbehandling og/eller helkroppsbestråling. Det foreligger hindring av blodsirkulasjonen i venesystemet i leveren på grunn av ødelagte blodkar. Alvorlig VOD er en sjelden tilstand som oftest ses innen 4 uker etter transplantasjonen.
Økning av enzymet transaminase på transplantasjonstidspunktet er assosiert med økt risiko for venookklusiv leversykdom. Første tegn er ofte langsom vektøkning og økt behov for tilførsel av blodplater. Pasienten kan ha sterke magesmerter, særlig i øverste del av buken (epigastriet og høyre hypokondrium), bilirubin og transaminasestigning og økende leverstørrelse med øm lever. Det kan tilkomme ascites med vektøkning, eventuelt mental svikt og koagulasjonsforstyrrelser. Ved langt utviklet sykdom kan pasienten utvikle hepatorenalt syndrom. Prognosen er dårlig ved alvorlig påvirkning av leveren.
Behandlingen er ekspektativ og symptomatisk, men det er rapportert god effekt av medikamentet defibrotide®. Pasientens tilstand må følges nøye, med overvåking av væske og elektrolyttbalanse.
Trombotisk mikroangiopati
Denne tilstanden forekommer sjelden, men det er en potensielt alvorlig komplikasjon, som rammer cirka 5 % av pasientene. Hvorfor tilstanden oppstår er bare delvis avklart, men skader på innsiden av blodårene står sentralt og har trolig sammenheng med ciklosporinbruk. Det forekommer flere undergrupper.
Symptomer er alvorlig nedbrytning av røde blodceller, nyresvikt, lavt antall blodplater, eventuelt nevrologiske symptomer på grunn av redusert sirkulasjon i de minste blodårene.
Behandlingsmessig avsluttes ciklosporin, som erstattes med andre immundempende legemidler. Plasmautskifting (det vil si at en stor mengde av blodet i kroppen skiftes ut) kan bli aktuelt, men effekten er sjelden god.
Les mer om andre sjeldne komplikasjoner
Tilbakefall etter allogen stamcelletransplantasjon
Ved tilbakefall etter transplantasjon for kronisk myelogen leukemi har det vist seg at tilførsel av T-lymfocytter fra donor gir ny komplett remisjon hos cirka 70 % av pasientene som har tilbakefall til kronisk fase. Denne effekten er ikke fullt ut dokumentert ved tilbakefall etter transplantasjon for akutt leukemi.